Ein nicht alltägliches Hemisyndrom
Abstract
Zusammenfassung. Ein Patient mit bekannter hereditärer hämorrhagischer Telangiektasie stellt sich aufgrund einer transienten rechtsseitigen Armschwäche und Schwindel vor. Aufgrund der Klinik und der Risikofaktoren wird die Diagnose einer transienten ischämischen Attacke gestellt. Im Verlauf erleidet der Patient ein Krampfereignis und fiebert zweimalig auf, ohne dass sich ein klarer Infektfokus zeigt. Die initiale Schädel-MRT zeigt eine zentroparietale Läsion links mit Zeichen eines Begleitödems. Aufgrund dieses ungewöhnlichen Begleitödems muss differenzialdiagnostisch auch an ein neoplastisches Geschehen gedacht werden. Die weiteren Untersuchungen zeigen jedoch keine Hinweise auf eine Neoplasie, die Verlaufs-MRT des Schädels dann jedoch das Bild septischer Embolien mit einem Hirnabszess. Nach neurochirurgischer Sanierung und entsprechender antibiotischer Behandlung zeigt sich ein erfreulicher klinischer Verlauf. Als Ursache der septischen Embolien fand sich eine pulmonale arteriovenöse Malformation im Rahmen der hereditären hämorrhagischen Teleangiektasie, die komplikationsfrei gecoilt werden konnte.
Abstract. A patient with known hereditary hemorrhagic telangiectasia presents with transient right arm weakness and dizziness. A transient ischemic attack is diagnosed on clinical and risk factors. In the course of the disease, the patient suffers a convulsive event and fever occurs twice without a clear focus on the infection. The initial skull MRI shows a centroparietal lesion on the left with signs of accompanying edema. Due to this unusual concomitant edema, a neoplastic event must also be considered for differential diagnosis. However, the further examinations show no evidence of neoplasia, but the course MRI of the skull shows the image of septic embolisms with a brain abscess. After neurosurgical remediation and appropriate antibiotic treatment, the clinical course is pleasing. The cause of the septic embolisms was a pulmonary arteriovenous malformation due to hereditary hemorrhagic telangiectasia, which could be coiled without complications.
Anamnese und Befunde
Ein bisher selbständiger 80-jähriger Patient präsentierte sich auf der Notfallstation, nachdem er während rund 15 Minuten eine transiente rechtsseitige Armschwäche und einen ungerichteten Schwindel erlebt hatte. Auf Nachfragen gab der Patient leichte frontale Kopfschmerzen an, sonst fiel die Systemanamnese unauffällig aus.
Bei uns im Hause war der Patient aufgrund rezidivierender Bluttransfusionen bei chronischer Epistaxis im Rahmen eines Morbus Osler-Weber-Rendu bekannt. Wegen einer peripheren arteriellen Verschlusskrankheit und einer Dyslipidämie wird er mit Atorvastatin behandelt.
Der Patient war bis anhin in einem guten Allgemeinzustand, ist verheiratet und auf keine externe Unterstützung angewiesen.
Bei Eintritt bestand eine hypertensive Gefahrensituation (BD 196/74 mmHg), der Patient war in allen Dimensionen orientiert und afebril. In der körperlichen Untersuchung fiel im Unterberger Tretversuch eine Abweichung nach rechts auf, weitere neurologische Defizite konnten nicht objektiviert werden. Die Inspektion zeigte multiple Teleangiektasien im Gesicht und über dem Rumpf. Laborchemisch fand sich eine chronische Anämie bei einem Hämoglobin von 85 g/l, das restliche Routinelabor mit Entzündungs-, Leber- und Nierenparametern war unauffällig. Ein EKG und Thorax-Röntgen ergaben keine Auffälligkeiten.
Die Angio-CT-Untersuchung des Schädels zeigte schwere arteriosklerotische Veränderungen der Halsgefässe, jedoch erfreulicherweise ohne relevante Stenosen und ohne Blutungshinweise. Wir hospitalisierten unseren Patienten mit der Verdachtsdiagnose einer TIA (transiente ischämische Attacke), auf eine Thrombozytenaggregationshemmung musste wegen der chronischen symptomatischen Epistaxis verzichtet werden.
Weitere Abklärungsschritte und Verlauf
Am nächsten Morgen kam es im Rahmen einer ausgeprägten Epistaxis und mit Husten zu einem Krampfereignis der oberen Extremitäten. Das Krampfereignis wurde von der Pflege beobachtet und dauerte wenige Minuten. In der anschliessenden klinischen Untersuchung imponierten eine Hypästhesie und ein Kraftdefizit (M3) des rechten Arms, eine Hemianopsie nach rechts, eine Dysarthrie und eine Gangataxie. Ein Meningismus wurde klinisch ausgeschlossen. In der anschliessenden Schädel-MRT-Untersuchung zeigte sich eine Läsion hochparietal links mit Zeichen eines Begleitödems. Zusätzlich fand sich ein alter Kleinhirninfarkt.
Differenzialdiagnostische Überlegungen
Aufgrund der Risikofaktoren [Dyslipidämie, PAVK (periphere arterielle Verschlusskrankheit), ausgeprägte atheromatöse Veränderungen der hirnzuführenden Gefässe] und des älteren zerebrovaskulären Infarktes stand die Verdachtsdiagnose einer frischen Ischämie im Vordergrund.
Allerdings machten uns die Radiologen darauf aufmerksam, dass bildmorphologisch bei einer solchen Läsion mit Begleitödem und raumforderndem Effekt (Abb. 1) eine Neoplasie nicht ausgeschlossen werden könne.
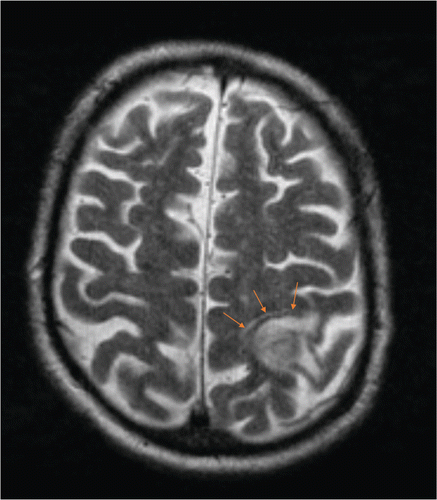
Ein EEG (Elektroenzephalografie) zeigte einen grossen Herdbefund, allerdings ohne Aktivitätszeichen. Wir starteten eine antiepileptische Abschirmung mit Levetiracetam und eine abschwellende Therapie mit Dexamethason.
Das anschliessend aufgetretene Fieber interpretierten wir im Rahmen einer Aspiration und begannen eine antibiotische Therapie mit Ceftriaxon.
Diagnose
Da es sich differenzialdiagnostisch um ein Tumorleiden handelte, wurde eine CT-Untersuchung vom Hals bis zum Becken im Sinne eines «Stagings» durchgeführt. Dabei fanden sich keine Auffälligkeiten, insbesondere auch keine Hinweise auf eine Aspirationspneumonie, sodass bei bereits wieder entfiebertem Patienten die antibiotische Therapie gestoppt werden konnte.
Drei Tage später erfolgte eine zerebrale Verlaufsbildgebung. Wir erhofften uns dadurch (MRT mittels Standard- versus Stroke-Protokoll) eine genauere Diagnostik der Läsion.
Dabei wies die unklare Läsion hochparietal links nach Kontrastmittelgabe ein umschriebenes Rand-Enhancement auf (Abb. 2). Dies passt einerseits zu einer Neoplasie, jedoch kommt differenzialdiagnostisch ein beginnender Hirnabszess in Frage. Da zusätzlich eine frische Ischämie okzipital links gesichtet wurde und der Patient erneut auffieberte, stand nun ein septisch-embolisches Geschehen im Vordergrund. Wir verlegten den Patienten mit dringendem Verdacht auf einen Hirnabszess ins Zentrumspital. Es wurde die Indikation zur Kraniotomie und Exploration gestellt, dabei konnte reichlich Eiter evakuiert werden, eine entsprechende Antibiotikatherapie wurde gestartet.
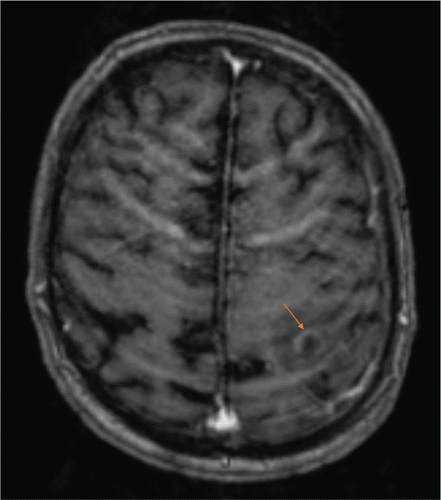
Der Patient wurde zu uns nach Thun zurückverlegt, nach Einlage eines peripheren Venenkatheters konnte eine intravenöse Antibiotikatherapie mit Ceftriaxon und Metronidazol im ambulanten Setting beendet werden. Die neurologischen Defizite zeigten sich erfreulicherweise bis auf eine Hypästhesie im Bereich des rechten Oberarms rückläufig. Der Erfolg der antibiotischen Therapie konnte auch in der Verlaufs-MRT nach drei Monaten objektiviert werden.
Da weder in der CT-Untersuchung (Hals-Thorax-Abdomen-Becken) noch in der Echokardiografie ein Fokus für das septisch-embolische Geschehen gefunden werden konnte, musste die Ursache der septischen Hirnembolien im Rahmen des Morbus Osler-Weber-Rendu interpretiert und gesucht werden. Bei unserem Patienten konnte retrospektiv eine pulmonale arteriovenöse Malformation (AVM) in der CT-Untersuchung dargestellt werden (Abb. 3). Die pulmonale AVM konnte im Verlauf komplikationsfrei mit einem Coil embolisiert werden.
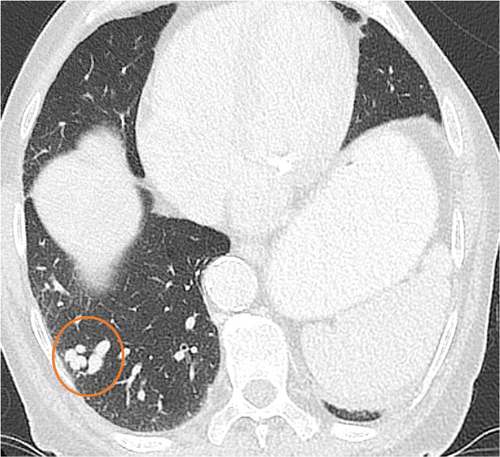
Kommentar
Der Morbus Osler-Weber-Rendu, auch hereditäre hämorrhagische Teleangiektasie (HHT) genannt, ist eine häufig unterdiagnostizierte, autosomal dominant vererbbare Gefässerkrankung mit einer Inzidenz von 1:5000 bis 1:8000. Die Krankheit kann sich in einer Vielfalt von klinischen Symptomen äussern, und das Manifestationsalter variiert von der Jugend bis ins hohe Alter. Die Diagnosestellung wird klinisch basierend auf den Curaçao-Kriterien (Tab. 1) gestellt [1].
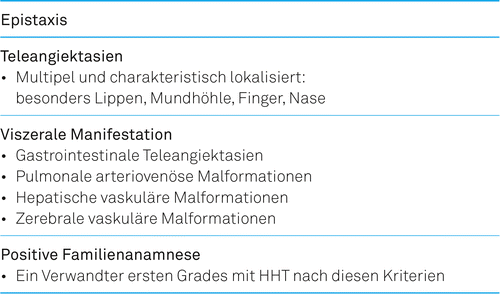
Zudem können auch genetische Tests Hinweise auf eine HHT liefern. Diese aufwändigen Tests eignen sich jedoch nicht als Screening. Sie finden nur bei Patienten Anwendung, die Familienangehörige mit bekannter HHT haben und selber «noch» nicht die klinischen Kriterien erfüllen. Ziel ist in diesen Situationen eine frühzeitige Diagnose einer HHT, um mögliche Komplikationen zu vermeiden [1].
In der Regel manifestiert sich eine HHT primär mit einer rezidivierenden Epistaxis, das durchschnittliche Manifestationsalter liegt dabei bei zwölf Jahren. Im weiteren Verlauf von 5–30 Jahren lassen sich bei den meisten HHT-Patienten Teleangiektasien im Mund, Gesicht oder an den Händen sehen [1].
Teleangiektasien im Magendarmtrakt führen aufgrund ihrer Vulnerabilität häufig zu einer Eisenmangelanämie. Neben den Teleangiektasien können arteriovenöse Malformationen auftreten, die die Ursache verschiedener schwerer Komplikationen sein können. Bei zerebralen AVM besteht das Risiko eines hämorrhagischen Strokes. Hepatische AVM können zu einem High-output-Problem mit Herzversagen und pulmonale AVM zu paradoxen zerebrovaskulären Embolien führen.
Bei unserem Patienten wurde die Diagnose im 30. Lebensjahr gestellt, nachdem seine Tochter im jugendlichen Alter plötzlich an einer Hirnblutung verstorben war. Die weiteren Abklärungen liessen dann auf eine rupturierte zerebrale arteriovenöse Malformation schliessen. Des Weiteren wurden bei unserem Patienten nach der Hospitalisation endoskopisch mehrere Teleangiektasien im Magendarmtrakt gesichtet, die sicherlich mitverantwortlich für die chronische Eisenmangelanämie waren. Hinweise auf eine hepatische AVM fanden sich weder im Angio-CT des Abdomens noch in der durchgeführten Echokardiografie.
In unserem Fall führte eine transiente Bakteriämie über die dargestellte Shuntverbindung der pulmonalen AVM zum Hirnabszess. Die Ursache der transienten Bakteriämie ist nicht ganz klar, am ehesten sehen wir dies im Rahmen der häufigen Nasentamponade bei reizidivierender Epistaxis. Dies ist bekannt und wurde bereits beschrieben [2]. In den mikrobiologischen Proben unseres Patienten konnte ein Streptococcus milleri nachgewiesen werden. Diese Gram-positiven Kokken gehören zur Normalflora des Nasopharyngeal- sowie des Gastrointestinaltrakts.
Neben der Abszessbehandlung muss unbedingt an die kausale Therapie bzw. an die Behandlung der pulmonalen AVM gedacht werden. Dabei steht die Embolisation der Shunts an vorderster Stelle. Die Indikation hängt einerseits vom Durchmesser der zuführenden Arterie, anderseits von der jeweiligen Symptomatik ab. Bei 15–50 % aller Patienten mit HHT lassen sich pulmonale AVM feststellen. Deshalb ist es wichtig, dass bei HHT-Patienten mit einem zerebrovaskulären Ereignis auch an gekreuzte Embolien, respektive an septische Embolien gedacht wird und in der Folge die pulmonalen AVM gesucht werden [1].
Patienten mit bekannten pulmonalen AVM, welche sich jedoch dem interventionell-radiologischen Verschluss entziehen, sollen vor Eingriffen mit Bakteriämieriskio eine Antibiotikaprophylaxe erhalten.
Die HHT-Guidelines empfehlen zudem, alle Patienten mit HHT drei- bis fünfjährlich mittels Computertomografie auf pulmonale AVM zu screenen. Zudem ist im Erwachsenenalter eine MRT des Hirns zur Suche nach arteriovenösen Malformationen indiziert [1].
- •Der Morbus Osler ist eine unterdiagnostizierte autosomal dominant vererbbare Gefässerkrankung.
- •Angiodysplasien führen häufig zu rezidivierender Epistaxis und gastrointestinalen Blutungen mit einer Eisenmangelanämie.
- •Die Diagnose «Morbus Osler» impliziert mehr als nur Nasenbluten und Hautveränderungen. Die arteriovenösen Missbildungen können zu schwerwiegenden Komplikationen führen: hämorrhagische Strokes, paradoxe zerebrale Embolien und Abszesse, Herzversagen. Patienten sollten auf diese AVM gescreent werden.
- •Bei Patienten mit bekanntem Morbus Osler und einem zerebrovaskulären Ereignis muss an eine gekreutze Embolie gedacht und die pulmonalen AVM müssen gesucht werden. Zudem sollte differenzialdiagnostisch ein Hirnabszess selbst bei normwertigen Entzündungszeichen in Betracht gezogen werden.
- •Die Diagnose wird klinisch anhand der Curacao-Kriterien gestellt.
Bibliografie
, : International guidelines for the diagnosis and management of hereditary hemorrhagic telangiectasia.
J Med Genet 2011; 48: 73–87., Zarkaria M: Infective endocarditis of native valve after anterior nasal packing. Am J Ther 2006; 13: 460–462.