Recommandations de Swiss Memory Clinics pour le diagnostic des démences
Abstract
Résumé. Le diagnostic précoce des atteintes cognitives, ressenties subjectivement ou rapportées par un tiers, est essentiel pour détecter des maladies neurodégénératives ou exclure des causes traitables telles que des pathologies de médecine interne, neurologiques ou psychiatriques. C’est la seule façon de garantir un traitement anticipé. Dans le cadre du projet 3.1 de la stratégie nationale en matière de démences 2014–2019 («Mise en place et extension d’un réseau de centres de compétences régionaux pour le diagnostic»), l’association Swiss Memory Clinics (SMC) s’est fixé pour objectif d’améliorer les normes de qualité en matière de diagnostic des démences et de soins de proximité dans ce domaine. Ces recommandations contiennent des directives d’ordre général sur le diagnostic et les différentes possibilités d’examens, et proposent des normes pour les procédures à appliquer. Elles expliquent en détail les différents éléments du diagnostic standard, tels que l’anamnèse, l’examen clinique, l’analyse de laboratoire, les tests neuropsychologiques et les procédures neuroradiologiques, et présentent des examens complémentaires pouvant alimenter les réflexions sur le diagnostic différentiel. Les principaux objectifs des recommandations SMC pour le diagnostic des démences sont les suivants: assurer l’accès à un diagnostic de haute qualité à un maximum de personnes atteintes, améliorer le diagnostic précoce de la démence, ainsi que proposer aux médecins de premier recours et aux collaborateurs de Memory Clinics un outil d’investigations diagnostiques utile.
Abstract. The early diagnosis of subjectively perceived or externally anamnestically observed cognitive impairments is essential for proving neurodegenerative diseases or excluding treatable causes such as internal, neurological or psychiatric disorders. Only in this way is early treatment made possible. As part of the project 3.1 of the National Dementia Strategy 2014–2019 (’Development and expansion of regional and networked centres of competence for diagnostics’), the association Swiss Memory Clinics (SMC) set itself the goal of developing quality standards for dementia clarification and improving the community-based care in this field. In these recommendations, general guidelines of diagnostics and individual examination possibilities are presented, and standards for the related processes are suggested. Individual areas such as anamnesis, clinical examination, laboratory examination, neuropsychological testing and neuroradiological procedures are discussed in detail as part of standard diagnostics, and supplementary examination methods for differential diagnosis considerations are portrayed. The most important goals of the SMC recommendations for the diagnosis of dementia are to give all those affected access to high-quality diagnostics, if possible, to improve early diagnosis of dementia and to offer the basic service providers and the employees of Memory Clinics a useful instrument for the clarification.
Zusammenfassung. Die Frühdiagnostik subjektiv wahrgenommener oder fremdanamnestisch beobachteter kognitiver Beeinträchtigungen ist essenziell, um neurodegenerative Erkrankungen nachzuweisen oder behandelbare Ursachen wie internistische, neurologische oder psychiatrische Störungen auszuschliessen. Nur dadurch wird eine frühzeitige Behandlung ermöglicht. Im Rahmen des Projekts 3.1 der Nationalen Demenzstrategie 2014–2019 («Auf- und Ausbau regionaler und vernetzter Kompetenzzentren für die Diagnostik») hat sich der Verein Swiss Memory Clinics (SMC) zum Ziel gesetzt, Qualitätsstandards für die Demenzabklärung zu entwickeln und die wohnortsnahe Versorgung in diesem Bereich zu verbessern. In den vorliegenden Empfehlungen werden allgemeine Richtlinien der Diagnostik und einzelne Untersuchungsmöglichkeiten vorgestellt, sowie Standards für die diesbezüglichen Abläufe vorgeschlagen. Einzelne Bereiche wie Anamneseerhebung, klinische Untersuchung, Laborparameter, neuropsychologische Testung und neuroradiologische Verfahren werden als Teil der Standarddiagnostik ausführlich diskutiert, ergänzende Untersuchungsmethoden für differenzialdiagnostische Überlegungen abgebildet. Die wichtigsten Ziele der SMC-Empfehlungen zur Diagnostik der Demenzerkrankungen sind es, möglichst allen Betroffenen Zugang zu einer qualitativ hochstehenden Diagnostik zu ermöglichen, die Frühdiagnostik der Demenz zu verbessern und den Grundversorgern sowie den Mitarbeitenden der Memory Clinics ein nützliches Instrument für die Abklärung anzubieten.
Abréviations utilisées dans l’article
AIVQ activités instrumentales de la vie quotidienne
ApoE apolipoprotéine E
ASNP Association suisse des neuropsychologues
AVQ activités de la vie quotidienne
BDI Beck Depression Inventory
CDT (carbohydrate deficient transferrin): transferrine désialylée
CERAD-NAB Consortium to Establish a Registry for Alzheimer’s Disease – Neuropsychological Assessment Battery
CIM-10 classification statistique internationale des maladies et des problèmes de santé connexes, 10e révision
CT ([cranial] computed tomography): scanner cérébral
DemTect test de détection de la démence
DSM-5 (Diagnostic and Statistical Manual of Mental Disorders): Manuel diagnostique et statistique des troubles mentaux, 5e édition
EEG électroencéphalogramme
GDS (geriatric depression scale): échelle de dépression gériatrique
GOT (glutamate oxaloacetate transaminase): transaminase glutamique oxalacétique
GPT (glutamate pyruvate transaminase): transaminase glutamique pyruvique
INR international normalized ratio
IRM cérébrale imagerie par résonance magnétique du cerveau
MCI (mild cognitive impairment): trouble cognitif léger
MCJ maladie de Creutzfeldt-Jakob
MMSE Mini Mental Status Examination
MoCA Montreal Cognitive Assessment
NOSGER Nurses’ Observation Scale for Geriatric Patients
OPAS ordonnance sur les prestations de l’assurance des soins
SCPD symptômes comportementaux et psychologiques de la démence
SMC Swiss Memory Clinics
SNC système nerveux central
SPECT (single photon emission computed tomography): tomographie par émission monophotonique
SPPA Société suisse de psychiatrie et psychothérapie de la personne âgée
SPSG Société professionnelle suisse de gériatrie
TEP tomographie par émission de positons
TSH (thyroid stimulating hormone): hormone thyréotrope
VIH virus de l’immunodéficience humaine
VS vitesse de sédimentation
γ-GT gamma-glutamyl transpeptidase
L’association Swiss Memory Clinics (SMC) s’engage – en tant que représentante des centres suisses de dépistage des démences – pour une qualité optimale du diagnostic et du traitement des démences sur l’ensemble du territoire suisse. Dans le cadre de la stratégie nationale en matière de démence 2014–2019, SMC a pris la direction du projet 3.1 «Mise en place et extension d’un réseau de centres de compétences régionaux pour le diagnostic». Un objectif essentiel du projet consiste à formuler des normes de qualité reconnues sur le plan suisse pour les examens de dépistage des démences. Ces normes devront contribuer à améliorer l’aptitude des professionnels de la santé à détecter une démence le plus tôt possible et à réaliser eux-mêmes ou à ordonner les étapes du diagnostic indiquées, ainsi qu’à donner accès aux personnes suspectées de démence à un diagnostic adéquat et de qualité, à proximité de leur domicile. Un concept de formation continue accompagnera l’introduction des normes de qualité de la SMC.
Un groupe de travail formé de membres des SMC, de représentants officiels de la Société suisse de psychiatrie et psychothérapie de la personne âgée (SPPA), de la Société professionnelle suisse de gériatrie (SPSG), de la Société suisse de neurologie (SSN), de l’Association suisse des neuropsychologues (ASNP) et d’experts des différentes disciplines ou institutions a préparé ces recommandations portant sur le diagnostic des démences. Elles visent à refléter l’état actuel des possibilités de diagnostic, à faire connaître les développements en la matière et à présenter succinctement les principaux outils de diagnostic. Le groupe d’experts tient en particulier à améliorer le diagnostic précoce des démences, et à proposer un manuel utile à la pratique clinique quotidienne.
Recommandations générales pour la procédure diagnostique, à l’attention du médecin de famille et de la clinique de la mémoire
Recommandations pour le médecin de famille:
Dépistage des cas («case finding»):
En lieu et place d’un dépistage universel à partir d’un certain âge (p.ex. au moyen de tests cognitifs), une stratégie de recherche de cas est recommandée. Le dépistage des cas vise les individus qui présentent des facteurs de risque ou des symptômes d’une possible pathologie démentielle (drapeaux rouges [red flags]). Il incombe au médecin de premier recours d’être attentif aux drapeaux rouges (voir figure 1 avec algorithme détaillé). Selon les cas, l’investigation diagnostique aura lieu au cabinet du médecin de famille ou dans une clinique de la mémoire. Si un patient affichant des symptômes de type drapeaux rouges refuse de se déplacer, il convient qu’un médecin ou un service de consultation gériatrique ou psychogériatrique lui rendent visite à domicile à cet effet. Il en va de même pour les résidents d’EMS présentant des symptômes de type drapeaux rouges.
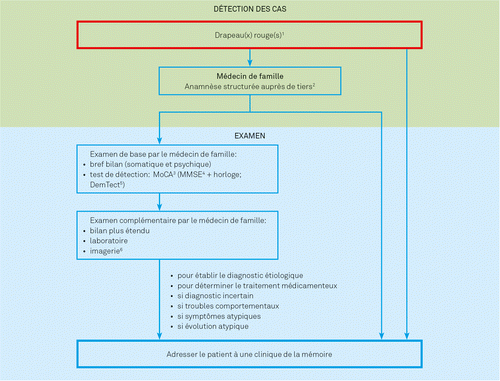
Le Mini Mental Status Examination (MMSE) figure souvent parmi les tests cognitifs réalisés dans les cabinets médicaux [1]. Le MMSE n’est hélas pas assez sensible pour détecter la démence à un stade précoce. D’où l’utilité, pour obtenir de meilleurs résultats, de compléter le MMSE par le test de l’horloge [2]. Le test de détection de la démence (DemTect) est également répandu en Suisse [3]. Mais de façon générale, il est recommandé d’opter pour l’évaluation cognitive de Montréal (Montreal Cognitive Assessment, MoCA) [4], en raison de sa sensibilité accrue, de sa mise à disposition gratuite dans différentes langues, et de ses résultats concluants dans la pratique.
Procédure à la clinique de la mémoire:
Investigations interdisciplinaires par des médecins (psychiatre de l’âge avancé, gériatre, neurologue – tous ces spécialistes font partie de l’équipe de la clinique de la mémoire, ou du moins sont en étroits contacts avec elle et prêts à intervenir en tout temps) et des neuropsychologues, év. par d’autres spécialises en médecine de la personne âgée (gérontologue, travailleur social, etc.):
- •Anamnèse et hétéro-anamnèse complètes, sur la base d’entretiens semi-directifs
- •Status psychique et somatique
- •Tests neuropsychologiques
- •Imagerie (neuroradiologie, év. médecine nucléaire)
- •Examen de laboratoire
- •Conférence interdisciplinaire avec diagnostic selon les codes CIM-10 ou DSM-5 (le codage sera toujours indiqué selon la liste CIM-10)
- •Le degré de gravité des troubles neurocognitifs selon le DSM-5 est fixé en fonction des conséquences invalidantes au quotidien:
- •léger: limitation des AIVQ seulement (activités instrumentales de la vie quotidienne) [5], p.ex. tenir son ménage, gérer son argent
- •moyen: limitation des AVQ de base (activités de base de la vie quotidienne) [6], p.ex. se nourrir, s’habiller
- •sévère: dépendance totale
- •Entretien diagnostique avec le patient et ses proches. Recommandations diagnostiques et thérapeutiques, et conseils au patient (p.ex. directives anticipées, mandat pour cause d’inaptitude, aptitude à conduire) ainsi qu’à ses proches (stratégies de résolution des problèmes dans le cadre familial, gestion des troubles comportementaux, possibilités de décharge)
- •Traitement médicamenteux (p.ex. médicaments pro-cognitif, prévention vasculaire, antidépresseurs, conseil en cas de comorbidités relevant de la psychiatrie, de la neurologie ou de la médecine interne)
- •Mise en place – ou proposition – de traitements non médicamenteux (p.ex. ergothérapie cognitive, entraînement cognitif en milieu de vie ou activités physiques stimulant les fonctions cognitives, musicothérapie, thérapie artistique, logopédie, etc.)
- •La clinique de la mémoire sert d’interlocuteur pour toutes les questions ou adaptations liées à l’évolution de la maladie: changements de comportement problématiques, ajustement des médicaments et des traitements, conseils aux proches (surmenage, sentiments de culpabilité), institutionnalisation, questions de droit des assurances et de droit médical.
Anamnèse médicale
Il est essentiel de documenter en détail la phase prodromique et les facteurs de risque, et de décrire le début de la maladie et son évolution avec ses éventuelles fluctuations, en distinguant bien entre la perception des faits propre au patient et celle de l’entourage. Une anamnèse familiale doit être effectuée et inclure l’âge et la cause de décès des parents, des frères et sœurs et le cas échéant des enfants. Les maladies diagnostiquées chez plusieurs membres de la famille doivent également être déterminées. S’il existe des cas de démence, les données concernant l’âge de début de la maladie et son évolution seront également notées. Par ailleurs, une anamnèse personnelle complète s’impose, notamment une anamnèse portant sur les médicaments, y compris l’automédication. Il convient de connaître en détail les médicaments pris la veille et le jour de l’examen (y compris les médications en réserve).
Anamnèse systématique
- •Substances nocives: alcool, nicotine, drogues, abus de médicaments
- •Système cardiovasculaire: troubles cardio-pulmonaires, arythmies cardiaques (fibrillation auriculaire notamment)
- •Alimentation: évolution du poids, alimentation, y compris état dentaire/dysphagie, digestion, troubles du transit (p.ex. constipation), régimes, diabète
- •Miction: incontinence urinaire, dysurie, mictions fréquentes et urgentes
- •Sensations: vertiges, céphalées, douleurs générales
- •Récupération: somnolence diurne, troubles de l’endormissement et du sommeil, cauchemars, agitation nocturne, parasomnies, ronflements, phases d’apnée
- •Mobilité: aides à la marche, chutes (fréquence, cause et déroulement), perte d’assurance dans les déplacements
- •Signes neurologiques: troubles de coordination et d’équilibre, tremblements, parésie, faiblesse générale (déclin de la motricité/sensibilité), aboulie, dysphagie, crampes, traumatisme craniocérébral
- •Langage: élocution difficile ou ralentie, peine à trouver ses mots, paraphasie
- •Organes sensoriels: baisse de la vision et de l’audition, altération du goût et de l’odorat
- •État psychique: symptômes dépressifs, tendances suicidaires, troubles anxieux, irritabilité, hallucinations
- •Anamnèse de délirium
- •Pour finir: troubles n’ayant pas encore été abordés.
Anamnèse psychosociale
Le diagnostic des démences intervient souvent chez des patients âgés, dont la capacité de communication est restreinte et dont la multimorbidité rend l’anamnèse d’autant plus difficile. Dans bien des cas, l’empathie témoignée lors d’un entretien minutieux avec présentation des troubles, saisie des problèmes et mise en évidence des liens soulagera déjà le patient et son entourage. Ceux-ci seront priés de décrire les anomalies, les gênes et les modifications intervenues au quotidien. Il semble ici déterminant de donner au patient et à ses proches la possibilité de décrire les difficultés rencontrées, sans se focaliser sur un problème précis. Cela permet notamment de se faire une idée des souffrances endurées, de la dynamique relationnelle et des ressources existantes.
Un entretien semi-structuré avec le patient et ses proches servira ensuite à l’anamnèse des problèmes dus aux troubles cognitifs vécus et observés au quotidien. Des questions ciblées porteront sur les performances mnésiques, les capacités de langage et de communication, l’aisance à planifier et gérer les tâches, ainsi que les capacités d’orientation dans le temps et l’espace. La gestion du quotidien, en particulier le degré d’autonomie dans les activités quotidiennes primaires (de base) ou étendues (instrumentales) sera abordée. Il s’agit de connaître le besoin d’aide, l’assistance requise ou les auxiliaires intervenant déjà. Des informations seront recueillies sur la conduite (sécurité et compétence au volant) et/ou l’utilisation des moyens de transport publics. Par ailleurs, il est recommandé de s’informer des activités sociales, des hobbies et des contacts entretenus. L’anamnèse fera notamment ressortir les divergences entre la version des faits rapportés par le patient et celle des tiers interrogés.
L’entretien sera complété par des questions précises portant sur la latéralisation, le langage primaire et élaboré, dans le cadre d’une anamnèse sociale concernant les aspects de la vie comme la formation, la carrière professionnelle, la situation de famille et la situation de vie actuelle. Aux anamnèses médicale et psychosociale s’ajoutent d’ordinaire des autoévaluations et des évaluations tierces, réalisées au moyen de différentes échelles:
- •Informant Questionnaire on Cognitive Decline in the Elderly (IQCODE)
- •Nurses’ Observation Scale for Geriatric Patients (NOSGER)
- •Caregiver Burden Inventory (CBI)
- •Neuro-Psychiatric Inventory (NPI)
- •Échelle de dépression gériatrique (GDS)
- •Epworth Sleepiness Scale (ESS)
Collecte de données sur les capacités au quotidien
À propos des activités de la vie quotidienne (AVQ), on distingue entre les AVQ de base et les activités instrumentales de la vie quotidienne (AIVQ). Les AVQ de base consistent à s’alimenter, se laver, s’habiller, aller aux toilettes, contrôler ses sphincters, se lever de son lit ou d’une chaise et se déplacer (avec ou sans aide à la marche). Les compétences suivantes font partie des AIVQ: préparer des repas, faire le ménage et la lessive, gérer son argent, téléphoner, faire ses achats, prendre ses médicaments et utiliser un moyen de transport.
La collecte des données sur la vie quotidienne d’un patient, dans le cadre de son anamnèse ou de l’anamnèse auprès d’un tiers, repose en principe sur quatre sources possibles:
- 1.Observation du patient dans le cadre d’un examen AVQ de base/AIVQ standardisé
- 2.Questionnaire standard soumis au patient
- 3.Questionnaire standard soumis aux proches ou aux accompagnants
- 4.Collecte de données lors d’une visite à domicile (chez le patient, au home, etc.)
Il faut toujours distinguer entre les capacités qui étaient celles du patient par le passé et ses capacités actuelles, et relever le décalage entre l’anamnèse et l’hétéro-anamnèse. Il peut être intéressant de savoir si la personne utilise les nouvelles technologies (AIVQ), ou si elle préfère ne pas s’aventurer en terrain inconnu.
La saisie standardisée, lors de l’anamnèse d’un tiers, des capacités présentes au quotidien est indispensable à la pose de tout diagnostic de démence. Jekel et al. [7] propose une synthèse complète des échelles – notamment pour les patients atteints d’un trouble cognitif léger (mild cognitive impairment, MCI). En Suisse, l’échelle NOSGER [8] et le questionnaire à 16 items sur le déclin cognitif des patients âgés rempli par le proche («Informant Questionnaire on Cognitive Decline in the Eldelry») [9] se sont établis. On trouve également en Suisse une version à 7 items validée [10].
D’autres instruments sont couramment utilisés en Suisse, comme l’échelle «The Lawton Instrumental Activities of Daily Living (IADL) Scale» [5] et l’indice «Index of Independence in Activities of Daily Living» [11]. Une révision systématique [7] n’a pas permis de déterminer de manière probante quelle AIVQ est la plus utile dans le diagnostic des MCI. Il semble cependant que certaines AIVQ nécessitant une performance cognitive supérieure (p.ex. gérer ses finances) et les activités demandant un savoir-faire technologique (p.ex. utilisation d’un téléphone mobile) étaient les plus prometteuses. Une autre échelle, l’«Alzheimer’s Disease Cooperative Study – Activities of Daily Living Inventory» [12], spécialement développée pour les études médicamenteuses, semble pertinente pour évaluer les changements.
ymptômes comportementaux et psychologiques de la démence (SCPD)
Outre les symptômes cognitifs, les patients atteints de démence présentent une série de symptômes psychiatriques et comportementaux qui compliquent le traitement et l’évolution de la maladie, ainsi que sa prise en charge [13]. Le terme de «symptômes psychologiques et comportementaux des démences» (SCPD) a été proposé par l’association internationale de psychogériatrie (International Psychogeriatric Association, IPA). Les SCPD sont lourds de conséquences, tant pour les patients que pour les proches aidants leur prodiguant des soins.
Standard
- •Évaluation de la présence et caractérisation des SCPD
- •Évaluation subjective par le patient
- •Hétéro-évaluation par un proche/soignant connaissant bien le patient
- •Evaluation du fardeau des SCPD pour les proches/soignants
- •Observation de l’interaction comportementale entre le patient et l’accompagnant
- •Pondération de l’information dans le processus diagnostique
- •Information sur les SCPD à l’usage du patient
- •Information sur les SCPD à l’usage des proches
- •Évaluation de la pertinence d’un transfert vers une consultation spécialisée (p.ex. psychogériatrie de consultation et de liaison) pour la prise en charge des SCPD.
Optionnel
- •L’utilisation d’échelles est recommandée: NPI-Q, NOSGER ou échelles équivalentes
- •Prise en charge des SCPD: prise en compte des recommandations des sociétés de discipline suisses [14]
- •Transfert à une consultation spécialisée pour avis et le cas échéant prise en charge des SCPD, notamment si les SCPD sont sévères, en cas de comorbidités psychiatriques suspectées ou connues, d’implications familiales complexes ou si la question d’éventuelles mesures de contrainte se pose.
Psychopathologie
Standard
- •Évaluation clinique de la présence d’une psychopathologie
- •Évaluation subjective sollicitée auprès du patient
- •Hétéroévaluation par un proche/soignant connaissant bien le patient, d’entente avec lui
- •Status psychopathologique de base
- •Capacité de diagnostiquer une comorbidité psychiatrique
- •diagnostic de trouble dépressif
- •diagnostic différentiel d’avec les pathologies affectives et psychotiques primaires
- •Pondération de l’information dans le processus diagnostique
- •Tenir compte des psychopathologies primaires dans les propositions thérapeutiques des troubles cognitifs, voire des SCPD
- •Recommander au médecin traitant de transférer les patients à des unités spécialisées, en particulier les policliniques psychogériatriques, lorsque:
- •les psychopathologies sont sévères
- •il y a une comorbidité psychiatrique sévère connue ou suspectée
- •il y a des implications familiales complexes
- •la question d’éventuelles mesures de contrainte se pose.
Optionnel
- •L’utilisation d’un canevas de description psychopathologique est recommandée:
- •L’utilisation d’échelles psychopathologiques spécifiques est recommandée:
- •
- •Prise en charge des psychopathologies concomitantes à la clinique de la mémoire:
- •en fonction des compétences et des disponibilités.
Tests cognitifs dans le cadre de l’examen neuropsychologique
Le principal apport des tests cognitifs lors d’un examen neuropsychologique réside dans la détection précoce et la quantification des dimensions cognitives atteintes. Un profil des forces et faiblesses cognitives constitue en outre une base importante pour la psycho-éducation, pour le conseil et un traitement adapté aux besoins des patients et de leurs proches. À l’instar de la présentation différenciée des troubles neurocognitifs du DSM-5 [17], l’examen neuropsychologique complet vise à fournir des indications tant qualitatives que quantitatives sur les six dimensions suivantes:
- •Attention complexe: attention soutenue, attention partagée, attention sélective, vitesse de traitement’
- •Fonctions exécutives: planification, prise de décision, mémoire de travail, analyse des retours/correction des erreurs, actions contre les habitudes/contraintes de comportement, flexibilité mentale;
- •Apprentissage et mémoire: mémoire immédiate, mémoire des faits récents (y c. rappel libre ou indicé et reconnaissance), mémoire à très long terme (sémantique, autobiographique), apprentissage implicite’
- •Langage: production langagière (y c. dénomination et recherche de mots, fluence verbale, grammaire et syntaxe), compréhension du langage’
- •Habileté perceptivo-motrice: activités visuo-perceptives, visuo-constructives, perceptivo-motrices, praxies, gnosies’
- •Cognition sociale: détection des émotions, capacité d’empathie (théorie de l’esprit).
L’évaluation des performances reposera sur:
- a)la capacité mesurée lors des tests (au moins deux méthodes de tests par domaine, p.ex. pour la mémoire verbale et visuelle), ainsi que
- b)l’observation/le questionnement.
Au moment de choisir les tests, il faut s’assurer qu’ils remplissent les critères requis et d’utiliser des normes adaptées à l’âge. Il est essentiel, pour le diagnostic des troubles subtils, de prendre en compte le niveau de formation. Afin de rendre les variables du test cognitif directement comparables, il est recommandé d’utiliser des valeurs standard (p.ex. valeurs chiffrées, classement en pourcentage, etc.). Pour juger de l’évolution de la maladie, on pourra utiliser des versions parallèles ou, le cas échéant, la mesure des variations (change scores).
Choix des méthodes de test adéquates
Le standard minimum requis est un bref test cognitif dont les résultats permettront de choisir la bonne option pour l’examen neuropsychologique approfondi, compte tenu des informations tirées de l’anamnèse, de l’hétéro-anamnèse et en particulier des AVQ de base et des AIVQ. Le MoCA [4] ou le MMSE [1] combiné au test de l’horloge [18] sont recommandés et font ainsi partie intégrante de la méthode rapide standardisée. Un test cognitif différencié s’avère superflu pour les patients atteints de démence avancée (p.ex. MMSE <15/30). Un examen neuropsychologique adapté, se concentrant sur les difficultés du quotidien, peut néanmoins être indiqué pour de tels patients, car il constitue un excellent point de départ pour les conseils et l’accompagnement des malades et de leurs proches. D’ailleurs, plus la maladie progresse et plus le besoin d’outils d’évaluation extérieure de la fonctionnalité au quotidien et de l’existence de SCPD se fait sentir dans le cadre du suivi et du traitement des patients.
Un examen neuropsychologique approfondi constitue la norme dans les cliniques de la mémoire, pour les patients dont les capacités cognitives ne sont pas (encore) gravement altérées. En Suisse alémanique, le «Consortium to Establish a Registry for Alzheimer’s Disease – Neuropsychological Assessment Battery (CERAD-NAB)», enrichi de tests mesurant la vitesse de traitement et les fonctions exécutives (CERAD-Plus), est une batterie de tests dûment standardisées et validées qui connaît un grand succès. En Suisse romande, des tests équivalents sont utilisés. On y trouve les évaluations suivantes: énumération d’animaux (fluence sémantique), dénomination d’images (dénomination visuelle), apprentissage d’une liste de mots (mémoire épisodique verbale– mesure de l’encodage), dessin de figures (capacités visuo-constructives), rappel d’une liste de mots (mémoire épisodique verbale – rappel), reconnaissance d’une liste de mots, rappel de figures (mémoire épisodique non verbale – rappel), mots en s (fluence littérale) et Trail Making Test, A et B (rapidité de traitement/flexibilité). Les documents de test de CERAD-Plus, possibilité d’évaluation incluse, sont proposés gratuitement aux professionnels sur le site www.memoryclinic.ch. Une liste plus complète de tests, en français également, est publiée sur le site www.swissmemoryclinics.ch.
Un tel examen standard sera complété par des instruments neuropsychologiques supplémentaires appropriés, en cas de niveau cognitif initial élevé, si des questions se posent à propos de l’aptitude à la conduite ou de la capacité de travail, ainsi que pour les formes de démence rares ayant des patterns de référence cognitifs spécifiques.
Examen de groupes de patients particuliers
L’examen est particulièrement complexe dans les cas suivants: (a) contexte d’immigration avec compétences linguistiques limitées dans la langue de l’examen (le cas échéant, il est judicieux et rentable à long terme de faire appel à un interprète interculturel)’ (b) déficits sensoriels pour lesquelles il n’existe généralement pas de normes de référence’ (c) troubles du développement intellectuel’ (d) haut potentiel’ (e) personnes très âgées (> 90 ans). Dans de telles conditions, l’examen cognitif et son interprétation s’avèrent en général très délicats. Il convient de les adapter au cas par cas, ce qui requiert une vaste expertise neuropsychologique. En outre, il faut toujours tenir compte des troubles somatiques et psychiatriques ou des médicaments entravant les capacités cognitives, qui peuvent créer un biais dans l’évaluation.
Méthode pratique
Dans le cadre de l’examen neuropsychologique, la méthode rapide s’emploie dans un premier temps car elle permet, en tenant compte des informations issues de l’anamnèse et de l’hétéro-anamnèse, de choisir la méthode et le niveau adéquats pour l’examen neuropsychologique complet. Par la suite, une évaluation cognitives personnalisée et complète sera réalisée sur la base d’hypothèses. La batterie de tests CERAD-Plus, ou tests équivalents en français susmentionnés, est recommandée pour cette étape. Le résultat du test rapide, associé aux informations concernant l’âge, le niveau de formation, les compétences linguistiques et le statut professionnel, permet de choisir une batterie de tests cognitifs complets appropriée, à l’aide d’un algorithme (figure 2). Des exemples de batteries de tests standards et complexes proposés à choix sur la base de l’algorithme figurent dans Beck et al. [19].
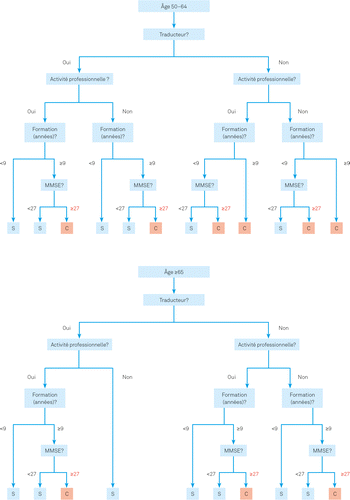
Évaluation, interprétation
Conformément au DSM-5, on parle de MCI (trouble neurocognitif mineur) lorsque la valeur standardisée d’au moins une dimension cognitive représente 1 à 2 écarts types par rapport à la moyenne (entre le 3e et le 16e percentile). En cas de trouble neurocognitif sévère (major neurocognitive disorder), la valeur standardisée doit s’élever à ≤ –2,0 (3e percentile ou moins) dans au moins une dimension. Il existe différentes méthodes pour calculer la valeur consolidée d’une dimension cognitive (p.ex. analyse des principaux composants). La classification du degré de gravité recommandée et compatible avec le DSM-5 est la classification en cinq catégories des «Directives en matière de classification et d’interprétation des résultats des tests neuropsychologiques» de l’Association suisse des neuropsychologues (ASNP)’ www.neuropsy.ch.
Rapport sur l’examen neuropsychologique
On se référera ici aux «Directives en matière d’établissement des rapports» de l’ASNP. L’évaluation neuropsychologique repose aussi bien sur des éléments quantitatifs et qualitatifs que sur l’observation du comportement et l’anamnèse (et hétéro-anamnèse). Le rapport devra indiquer en toute transparence le type de données sur lesquelles reposent les conclusions. En outre, il convient de prendre brièvement position sur le tableau clinique (p.ex. état de conscience, orientation, coopération/application dans les tâches, comportement social, comportement en entretien, expression spontanée, compréhension du langage et des instructions, motivation, rythme de travail, persévérance, mode de planification adopté, contrôle des erreurs, facteurs entravant les tests, conscience des troubles, etc.). Il est très utile de représenter dans un graphique, dans la mesure du possible, les résultats des tests cognitifs sur la base des six dimensions cognitives selon le DSM-5. Il est encore judicieux et souhaitable – sur la base des résultats des tests cognitifs et de réflexions d’ordre fonctionnel et neuro-anatomique – d’envisager les hypothèses relatives à l’étiologie d’un trouble existant. Les réflexions sur l’étiologie concrète et le diagnostic différentiel n’ont évidemment de sens qu’à condition d’y intégrer toutes les données recensées dans la clinique de la mémoire.
Examen somatique
Le status somatique est régi par la comorbidité et le diagnostic préliminaire (élément principal du questionnaire) et doit être adapté en conséquence (tableau 1).
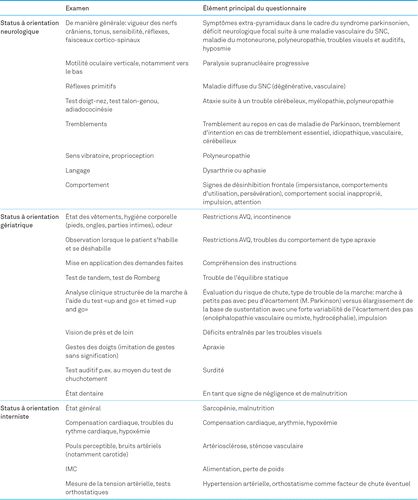
Diagnostic sanguin
Examen de base
- •Formule sanguine, protéine C-réactive
- •Glucose, HbA1c
- •Sodium, potassium, calcium
- •Créatinine
- •GOT (transaminase glutamique oxalacétique), GPT (transaminase glutamique pyruvique), γ-GT (gamma-glutamyl-transpeptidase)
- •TSH (hormone thyréotrope)
- •Vitamine B12, acide folique, vitamine D
- •Cholestérol, cholestérol HDL, triglycérides (statut lipidique chez les moins de 80 ans)
- •Syphilis et borréliose (en cas de soupçon)
Diagnostic de laboratoire en option
- •Électrocardiogramme
- •Hématologie différentielle, VS (vitesse de sédimentation), INR (international normalized ratio), créatine kinase, urée, acide urique, bilirubine
- •Profil du glucose sanguin
- •Hormones thyroïdiennes libres (T3, T4), parathormone, cortisol
- •Taux de vitamines B1, B6, niacine, homocystéine
- •Ferritine, transferrine, phosphate, chlorure, magnésium, zinc
- •Cuivre, céruloplasmine, examen d’urine avec clairance du cuivre dans les urines de 24h
- •VIH (virus de l’immunodéficience humaine)
- •CDT (transferrine carboxy-déficiente)
- •Dépistage des substances toxiques (plomb, mercure)
- •Dépistage de médicaments/drogues (p.ex. benzodiazépines)
- •Suivi des substances psychotropes
- •Anticorps des encéphalites auto-immunes ou paranéoplasiques (p.ex. anti-Hu, anti-Ma2, anti-CRMP5, anti-NMDA, etc.)
- •Paramètres des vasculites (notamment ANA, ANCA et RF’ en cas de suspision d’un syndrome bien défini, tests plus poussés, p.ex. facteurs C3 et C4 du complément, complexes immuns circulants, cryoglobulines, anti-DNS, anti-SSA, anti-SSB, etc.)
- •Génotypage de l’ApoE (apolipoprotéine E) (p.ex. dans le cadre de la recherche)
Diagnostic du liquide céphalo-rachidien (LCR)
Indications nécessitant un examen de LCR
- •Exclusion des formes autres que les démences primaires dégénératives, à l’instar notamment des maladies inflammatoires chroniques du SNC
- •Etayage de diagnostic des démences à progression rapide (notamment maladie de Creutzfeldt-Jakob (MCJ)
- •Ponction diagnostique ou de décharge, en cas de soupçon d’hydrocéphalie à pression normale
- •Diagnostic de soutien en présence d’une indication clinique spécifique de la maladie d’Alzheimer à un stade précoce, en cas d’évolution atypique de cette maladie et/ou si la maladie d’Alzheimer se déclare à un âge précoce (présénile)
Le tableau 2 résume le diagnostic de base du liquide céphalo-rachidien. En cas d’indication clinique, il convient de déterminer encore le taux d’immunoglobines IgA (plage de référence <5,00 mg/l) et IgM (plage de référence: <1,00 mg/l). En cas de suspicion clinique et de résultat positif dans le sérum, un diagnostic sérologique sera établi pour les borrélioses et la syphilis, et le cas échéant pour d’autres dosages sérologiques. Par ailleurs, une méthode de diagnostic précoce et différencié qui s’impose toujours plus consiste à déterminer le peptide amyloïde bêta, le phospho-tau et la protéine tau, en tant que biomarqueurs pour les démences.

Imagerie diagnostique
Les examens par imagerie du cerveau réalisés dans le cadre du diagnostic des démences remplissent deux fonctions essentielles:
- 1.exclure la présence d’une masse, les troubles de circulation du LCR, ainsi que les modifications d’origine vasculaire, métabolique ou inflammatoire’
- 2.contribuer à la différenciation étiologique et à la classification des formes primaires de démence.
Dans 5 % des cas de démence, un examen par imagerie révèle une cause non dégénérative et potentiellement guérissable (p.ex. hématome sous-dural, tumeur, hydrocéphalie à pression normale, pathologies vasculaires et inflammatoires) [20]. Or, de simples procédures d’analyse clinique ne sont pas assez sensibles pour exclure de tels tableaux cliniques, comportant des symptômes évocateurs d’une démence.
Standard
L’imagerie structurelle par résonance magnétique (IRM) ou, en cas de contre-indication, par scanner cérébral (CT) avec administration d’un produit de contraste, fait partie des méthodes standards de diagnostic. Un examen par imagerie s’impose si un ou plusieurs des critères suivants sont remplis [21, 22]:
- •patient de moins de 65 ans atteint de troubles cognitifs’
- •symptômes cognitifs (débuts aigus ou subaigus)’
- •démence à progression rapide’
- •traumatisme crânien craniocérébral révélé par l’anamnèse récente’
- •symptômes neurologiques focaux récemment apparus (p.ex. convulsions, incontinence, troubles de la marche, apathie etc.)’
- •apparition récente de symptômes neurologiques focaux (p.ex. réflexes pathologiques, hémiparésie, troubles de la vue)’
- •affection cancéreuse révélée par l’anamnèse (carcinomes métastatiques notamment)’
- •prise d’anticoagulants ou troubles de la coagulation sanguine’
- •symptômes cognitifs atypiques (p. ex. aphasie s’aggravant très vite, changements d’attitude, anomalies du comportement social);
- •évolution atypique de la démence.
L’imagerie cérébrale peut contribuer au diagnostic et au diagnostic différentiel entre la maladie d’Alzheimer et d’autres démences (p.ex. fronto-temporales), bien qu’à l’heure actuelle elle ne suffise pas à trancher entre ces étiologies [23]. L’imagerie structurelle est d’une grande utilité pour repérer l’emplacement des lésions intracérébrales et pour en estimer le nombre [24, 25]. Ainsi, l’imagerie doit être reconnue pour son apport à l’évaluation globale et à la classification des tableaux cliniques des démences, en combinaison avec l’anamnèse et les résultats tant cliniques que neuropsychologiques. Cela vaut notamment pour l’établissement du diagnostic différentiel entre les démences dégénératives, vasculaires ou mixtes.
Imagerie par résonance magnétique du cerveau (IRM cérébrale)
Le choix se portera plutôt sur le résultat de l’IRM, notamment pour les jeunes patients et en cas de symptômes à progression rapide, en raison de l’absence d’exposition au rayonnement et parce que la résolution des images anatomiques est bien meilleure qu’avec un CT. Une IRM se justifie en cas de suspicion clinique de maladie inflammatoire, tumorale ou métabolique.
Protocole d’examen (recommandation minimale)
Standard
- •IRM 3D pondérée en T1, acquisition sagittale du cerveau complet
- •econstitutions en trois dimensions
- •plan coronal, perpendiculaire à l’axe longitudinal du lobe temporal: évaluation de l’hippocampe et des régions temporales mésiales
- •plan sagittal: évaluation de l’atrophie pariétale et post-centrale
- •FLAIR transversal ou FLAIR 3D du cerveau complet
- •évaluation des lésions de la substance blanche et de l’atrophie corticale globale
- •T2-w TSE, coupe transversale du cerveau complet:
- •lésions de la substance blanche et infarctus lacunaires
- •T2*-w ou SWI:
- •microhémorragies, calcifications, dépôts de fer
- •DWI/ADC:
- •infarctus lacunaires subaigus’ MCJ
Optionnel
- •IRM 3D/VIBE T1 FS avec agent de contraste
- •reconstitutions en trois dimensions
- •Analyses volumétriques
Tomodensitométrie du cerveau (scanner cérébral, CT)
Faute d’IRM ou en cas de contre-indication (p.ex. stimulateur cardiaque, implants numériques, claustrophobie majeure), on procédera en premier lieu à un scanner cérébral (CT). Le CT sans produit de contraste est en règle générale suffisant pour confirmer ou exclure la présence d’un hématome sous-dural ou d’une hydrocéphalie, et avec certaines réserves pour identifier une démence vasculaire. Le CT se prête en revanche moins bien au diagnostic d’une maladie d’Alzheimer ou au diagnostic différentiel des formes de démence sous-corticale [21].
Protocole d’examen
Examen d’ordinaire natif (adjonction d’un produit de contraste en cas de suspicion clinique de présence d’une masse ou de processus vasculaire, en l’absence de contre-indication aux agents de contraste iodés).
Coupe CT axiale réalisée en mode hélicoïdal entre la base du cerveau et le vertex.
Reconstitutions dans la fenêtre tissus mous, p.ex. 3/3 mm:
- •plan transversal, parallèle à l’axe longitudinal du lobe temporal
- •plan coronal, perpendiculaire à l’axe longitudinal du lobe temporal
Sonographie des vaisseaux irriguant le cerveau
En cas de démence vasculaire ou de formes mixtes de démence vasculaire et dégénérative, il peut être pertinent d’évaluer par échographie Doppler ou duplex les sténoses des vaisseaux cérébraux [26].
Techniques de médecine nucléaire
Tomographie par émission de positons (TEP) au fluordésoxyglucose (18F) (TEP–FDG)
Dans la TEP-FDG, le métabolisme régional du glucose est représenté en images et comparé avec des valeurs normales. La TEP-FDG est la technique d’imagerie de médecine nucléaire la plus utilisée dans le diagnostic des démences. Les indications recommandées de la TEP-FDG sont résumées dans le tableau 3. Une application clinique fréquente de la TEP-FDG du cerveau concerne le dépistage précoce de la maladie d’Alzheimer, qui constitue la forme de démence la plus fréquente. Pour cette indication, la TEP-FDG offre un degré de fiabilité diagnostique élevé parmi les processus non invasifs. En effet, l’introduction d’une analyse statistique basée sur les voxels a permis d’augmenter sensiblement la précision diagnostique [27]. Aujourd’hui, un logiciel d’évaluation correspondant est proposé dans le commerce par différents fabricants, et l’évaluation statistique basée sur les voxels du TEP-scan est considérée comme l’élément essentiel du diagnostic TEP actuel des cas de démence.

La TEP-FDG présente une sensibilité supérieure pour la mise en évidence de modifications fonctionnelles comme organiques (neurodégénératives) du traitement cortical des informations. Elle convient parfaitement au dépistage précoce dans le cadre du diagnostic des déficits cognitifs, par exemple lorsque des cas de troubles cognitifs sont déjà objectivables mais ne correspondent pas entièrement aux critères formels de démence. Dans une méta-analyse, une sensibilité moyenne très élevée et une spécificité pour le diagnostic de la maladie d’Alzheimer a été calculée [28]. La TEP-FDG permet un pronostic à fiabilité élevée concernant la probabilité qu’un trouble cognitif léger (MCI) se transforme en maladie d’Alzheimer [29]. Lla corrélation anatomo-clinique des aires présentant un dysfonctionnement permet par ailleurs, dans de nombreux cas, de différencier les chevauchements cliniques de symptômes éventuels évoquant une neurodégénérescence précoce d’une atteinte fonctionnelle ressemblant à la démence (p.ex. en cas de maladie psychiatrique) et de troubles cognitifs d’origine différente (p.ex. encéphalite limbique). Le schéma localisationnel des aires hypométaboliques dans la TEP-FDG correspond au phénotype clinique de la maladie d’Alzheimer (p.ex. trouble mnésique, sémantique ou visuo-spatial prédominant) [30].
Il existe également des patterns métaboliques typiques pour plusieurs démences neurodégénératives moins fréquentes pouvant être différenciées grâce à la TEP-FDG. Cela concerne notamment la démence à corps de Lewy et diverses formes de dégénérescences lobaires fronto-temporales [31], dont notamment l’aphasie primaire progressive (forme sémantique, non fluente et logopénique) et l’atrophie corticale postérieure.
Pour résumer, la TEP-FDG est l’imagerie moléculaire de premier choix pour le diagnostic des démences neurodégénératives. Elle est aujourd’hui associée à la TEP/CT avec une tomodensitométrie (CT) effectuée selon une technique low-dose, où la CT sert à l’orientation anatomique et corrige les atténuations de la TEP. Il n’est généralement pas nécessaire d’effectuer une imagerie morphologique préalable (CT avec produit de contraste, IRM), qui sera réalisée indépendamment de la TEP-FDG. En outre, les dernières technologies de pointe disponibles parviennent à associer la TEP et l’IRM. L’examen IRM diagnostique y est effectué en même temps que la TEP-FDG. Car en cas de démences vasculaires ou non dégénératives, la TEP-FDG n’est pas suffisante comme procédure d’imagerie, et donc doit toujours être combinée à un examen IRM pour confirmer ou infirmer cette hypothèse diagnostique.
Conditions pour la prise en charge des coûts d’une TEP-FDG
Selon l’ordonnance sur les prestations de l’assurances des soins (OPAS), les coûts de la TEP-FDG sont pris en charge à condition que:
- 1.elle soit prescrite par un spécialiste en gériatrie, psychiatrie ou neurologie,
- 2.l’âge du patient n’excède pas 80 ans,
- 3.le début de la démence ne remonte pas à plus de 5 ans,
- 4.la valeur obtenue au MMSE ne soit pas inférieure à 10 points, et
- 5.qu’aucune TEP ou SPECT (tomographie par émission monophotonique) n’ait encore été effectuée.
Normes de réalisation de la TEP-FDG
- •Réalisation dans les centres TEP satisfaisant aux directives administratives du 20 juin 2008 de la Société suisse de médecine nucléaire (SSMN) (OPAS, annexe 1, ch. 9.2).
- •Normalisation spatiale du TEP-scan sur un atlas standardisé du cerveau et analyse statistique basée sur les voxels du métabolisme régional du glucose par rapport à un collectif normal.
- •Intégration de l’analyse statistique dans la documentation d’imagerie et le rapport de la TEP.
SPECT visant à déterminer la densité du transporteur de la dopamine au niveau du striatum à l’aide du marqueur 123I-Ioflupane (DaTSCAN®)
Le DaTSCAN® est un examen de médecine nucléaire visant à déterminer l’intégrité des terminaisons nerveuses dopaminergiques dans le striatum. Typiquement, en cas de syndromes parkinsoniens, on constate ici un résultat pathologique avec carence en dopamine. Les coûts d’une SPECT cérébrale au DaTSCAN® sont remboursés conformément à la liste des spécialités avec limitation de l’OFSP dans certains cas en vue de différencier le tremblement essentiel des syndromes parkinsoniens. Des preuves toujours plus nombreuses démontrent que le DaTSCAN® permet de distinguer avec une très grande fiabilité le type de démence à corps de Lewy (avec résultat pathologique de la SPECT concernant le transporteur de la dopamine) des autres formes de démences (en particulier la maladie d’Alzheimer avec résultat normal de la SPECT concernant le transporteur de la dopamine) [32]. Il en va de même pour la TEP utilisant le traceur 18F-Fluorodopa (18F-DOPA-TEP), méthode équivalente sinon supérieure pour déterminer la disponibilité cérébrale en dopamine [33].
TEP amyloïde
La TEP amyloïde permet de mettre en évidence la présence ou l’absence de plaques bêtaamyloïdes dans le cerveau. L’examen est réalisé à l’aide de différents marqueurs qui se lient à ces plaques. L’Amyvid® (florbétapir) et le Vizamyl® (flutémétamol) sont actuellement autorisés en Suisse. Les caisses-maladie ne sont toutefois pas tenues de rembourser ces prestations.
Des recommandations internationales ont été publiées sur l’utilisation clinique de cette technologie [34]. À l’heure actuelle, cet examen sert essentiellement aux investigations scientifiques, notamment dans le cadre de la recherche de processus pathologiques et en tant qu’examen d’inclusion pour des études médicamenteuses. Quand de nouveaux médicaments seront disponibles, un plus large domaine d’application clinique émergera.
Génétique
Les questions en lien avec la génétique des démences préoccupent souvent les personnes côtoyant un proche avec une pathologie démentielle [35]. Or ces questions sont bien plus fréquentes que le besoin effectif d’une consultation génétique spécialisée.
Standard
Les professionnels d’une clinique de la mémoire devront être en mesure de:
- •repérer les cas de démence familiale’
- •pondérer l’information dans le processus diagnostique’
- •poser l’indication d’une consultation génétique spécialisée’
- •documenter le cas et collaborer avec le spécialiste en génétique’
- •discuter avec le patient/les proches de l’éventuel transfert du cas à une consultation génétique’
- •transférer le patient/la famille à cette unité, habituellement localisée dans un service universitaire. Un transfert aura lieu notamment dans les cas suivants:
- •un apparenté au 1er degré possiblement atteint et âgé de moins de 50 ans’
- •deux apparentés au 1er degré possiblement atteints et âgés de moins de 60 ans’
- •renseigner et conseiller à propos de la génétique en tant que facteur de risque des pathologies démentielles les plus fréquentes’
- •donner des informations appropriées sur les facteurs de risque génétique.
Optionnel
- •Évaluation de la présence d’une éventuelle hérédopathie cognitive en utilisant un génogramme.
- •Consultation génétique, si la consultation de la mémoire possède l’expertise requise.
Autres examens
Les examens regroupés dans cette section complètent les mesures indiquées dans les recommandations générales pour la procédure diagnostique. Ils peuvent être utiles à l’évaluation par diagnostic différentiel du syndrome démentiel et/ou indiquer d’importantes maladies secondaires susceptibles d’influencer la manifestation clinique ainsi que le degré de gravité d’une pathologie démentielle. La décision en faveur de l’un des examens énumérés ci-dessous repose en général soit sur les indications déterminantes dans le cadre de l’anamnèse, soit sur les résultats du status somatique.
Électroencéphalographie (EEG)
L’électroencéphalographie est un procédé d’investigation peu contraignant et peu coûteux. Typiquement, on note avec la progression de la maladie d’Alzheimer ou de la démence à corps de Lewy un ralentissement de l’activité cérébrale de base. En revanche, l’activité basique paraît souvent normale chez les patients présentant une dégénérescence lobaire fronto-temporale. En conséquence de la sensibilité et de la spécificité toujours plus élevées des méthodes d’imagerie structurelle et fonctionnelle ainsi qu’analytiques en laboratoire, l’EEG ne joue plus qu’un rôle secondaire dans le diagnostic des démences.
Une investigation par EEG est susceptible de fournir des informations utiles en cas de:
- •variations importantes dans la vigilance et l’orientation, en vue de l’exclusion d’une origine épileptique’
- •suspicion d’une maladie inflammatoire/infectieuse, inflammatoire/auto-immune ou du SNC (p.ex. encéphalite limbique, encéphalopathie de Hashimoto), ainsi qu’en cas de suspicion de la maladie de Creutzfeldt-Jakob.
Diagnostic du trouble du sommeil
Les démences sont souvent accompagnées d’un besoin accru de sommeil, autrement dit d’un sommeil nocturne prolongé et d’une somnolence diurne accrue. Une telle somnolence diurne excessive peut être évaluée simplement, au moyen du questionnaire de somnolence d’Epworth qui mesure la tendance à s’endormir (> 9 points) ou du test du maintien de l’éveil, ou encore du test itératif de latence à l’endormissement (MWT, MSLT). Tout comme les maladies organiques du cerveau, les troubles respiratoires pendant le sommeil peuvent perturber l’architecture du sommeil et induire une somnolence diurne excessive, ainsi qu’une restriction des capacités de l’attention. Ils représentent un facteur de risque indépendant pour des événements cardio-vasculaires et cérébro-vasculaires et sont souvent traitables.
La réalisation d’un examen par appareillage au cours du sommeil (actimétrie, pulsoximétrie nocturne, polygraphie, polysomnographie) peut être indiquée en cas de:
- •somnolence diurne excessive et de signes de troubles respiratoires nocturnes (ronflement irrégulier, pauses respiratoires, détresse respiratoire nocturne, bouche sèche au réveil, sommeil non réparateur, etc.), en vue de l’exclusion d’un syndrome d’apnée du sommeil. L’obésité et la consommation régulière d’alcool en soirée augmentent le risque d’un trouble respiratoire pendant le sommeil’
- •suspicion d’un trouble du comportement au cours du sommeil paradoxal, dans le cadre de suspicion d’une maladie de Parkinson ou à corps de Lewy’
- •suspicion de crises épileptiques liées au sommeil.
Test de l’odorat
La maladie d’Alzheimer ainsi que la maladie de Parkinson impliquent précocement des altérations histopathologiques dans la région du cortex olfactif, y compris le cortex entorhinal. Leur corrélat clinique typique se manifeste par une baisse de l’odorat qui peut indiquer un développement de la maladie d’Alzheimer (ou de Parkinson), tant chez les patients plutôt âgés en bonne santé que chez ceux qui présentent de légers troubles cognitifs.
- •Un test de l’odorat peut fournir un résultat corroborant le diagnostic préliminaire lors du dépistage précoce de la maladie d’Alzheimer. Différents tests validés sont à disposition (tiges de test de l’odorat, Brief Smell Identification Test, etc.).
Analyse de la marche
Les pathologies neurodégénératives peuvent altérer, en plus de la cognition, les fonctions motrices. Beaucoup de personnes affectées par une démence présentent, par rapport aux sujets du même âge en bonne santé, un risque de chute accru. D’où l’utilité d’une analyse clinique structurée (test «up and go» évaluant la marche selon des critères standardisés) pour déterminer l’assurance à la marche et les risques de chute. Elle permet de juger de l’influence du contrôle central ainsi que d’autres facteurs somatiques (musculosquelettiques, neurologiques, sensoriels) sur les troubles de la locomotion. Elle montre dans quelle mesure des mesures thérapeutiques ou préventives adéquates (entraînement, auxiliaires de marche, etc.) sont indiquées. L’analyse quantitative de la marche repose sur des tests cliniques validés de la mobilité (p.ex. test «timed up and go»), mais aussi sur des procédés informatisés (les données de mobilité étant saisies numériquement, p.ex. au moyen de capteurs de pression sur le tapis de marche).
Oculomotricité/Champ de vision
Un examen clinique de l’oculomotricité et du champ de vision s’impose en cas de suspicion de certaines maladies neurodégénératives (p.ex. paralysie supranucléaire progressive) ou de pathologie vasculaire. Un examen par appareillage est en règle générale uniquement indiqué en cas d’investigation ciblée (p.ex. déficit des saccades oculaires, dégradation du champ visuel, acuité visuelle en cas de troubles peu clairs de la vue).
- •Dépistage des cas et non dépistage systématique: il incombe au médecin de premier recours d’être attentif précocément aux indices spécifiques, les symptômes et les facteurs de risque (drapeaux rouges) de démence.
- •Le MoCA est recommandé dans la pratique comme test cognitif de base, notamment lors de l’apparition des premiers symptômes ou d’un léger trouble de la cognition. Le MMSE/test de l’horloge ou le DemTect restent par ailleurs possibles. À la clinique de la mémoire, l’examen neuropsychologique repose sur la batterie de tests CERAD-Plus ou tests équivalents.
- •L’anamnèse et l’hétéro-anamnèse structurées, un examen clinique avec mesure de l’autonomie dans les activités quotidiennes, les tests neuropsychologiques, le diagnostic sanguin et l’imagerie structurelle constituent les étapes standard de toute investigation de la démence.
- •L’anamnèse et les examens cliniques prendront également en compte les symptômes comportementaux et psychologiques de la démence (SCPD).
- •Les examens en laboratoire servent principalement à exclure les causes de troubles cognitifs susceptibles d’être traités. La détermination des biomarqueurs joue un rôle toujours plus important.
- •L’IRM cérébrale est la méthode d’examen privilégiée en imagerie structurelle. Faute de pouvoir réaliser une IRM, un scanner cérébral (CT9) est indiqué.
- •Les techniques de médecine nucléaire sont indiquées lors de l’apparition de troubles neurodégénératifs ou pour les troubles cognitifs à l’étiologie indéfinie.
Questions de compréhension
- 1.Lequel des examens ci-dessous constitue-t-il la norme dans l’investigation de la démence ?
- a)Examen clinique avec mesure de l’autonomie dans les activités quotidiennes
- b)Test neuropsychologique
- c)Diagnostic sanguin
- d)Imagerie structurelle
- e)Tous
- 2.Laquelle des affirmations suivantes est-elle erronée ?
- a)Pour le dépistage de la démence, le dépistage des cas prime sur des examens systématiques.
- b)Le dépistage des drogues fait partie des examens de base.
- c)Le test MoCA, et à la clinique de la mémoire le test CERAD (ou équivalent), sont recommandés dans la pratique en tant qu’éléments-clés de la neuropsychologie.
- d)L’IRM est la méthode d’examen adoptée pour l’imagerie structurelle.
- e)Les techniques de médecine nucléaire s’utilisent pour les troubles cognitifs à l’étiologie indéfinie.
- 3.Le diagnostic du liquide céphalo-rachidien est absent de l’examen standard d’une des indications ci-dessous. Laquelle ?
- a)Exclusion des formes autres que les démences primaires dégénératives
- b)Démences à progression rapide
- c)Maladies cancéreuses
- d)Dérivation en cas d’hydrocéphalie à pression normale
- e)Démence à l’évolution atypique
Réponses aux questions:
La réponse correcte est e).
La réponse correcte est b).
La réponse correcte est c).
Bibliographie
: «Mini-mental state». A practical method for grading the cognitive state of patients for the clinician. J Psychiatr Res 1975; 12: 189–198.
, : Dementia screening in general practice: Optimized scoring for the Clock Drawing Test. Brain Aging 2002; 2: 36–43.
, : DemTect: a new, sensitive cognitive screening test to support the diagnosis of mild cognitive impairment and early dementia. Int J Geriatr Psychiatry 2004; 19: 136–143.
, : The Montreal Cognitive Assessment, MoCA: a brief screening tool for mild cognitive impairment. J Am Geriatr Soc 2005; 53: 695–699.
: Assessment of older people: self-maintaining and instrumental activities of daily living. Gerontologist 1969; 9: 179–186.
: Repeatability and validity of a modified Activities of Daily Living (ADL) Index in studies of chronic disabilty. Int Rehab Med 1979; 1: 51–58.
, : Mild cognitive impairment and deficits in instrumental activities of daily living: a systematic review. Alz Res Therapy 2015; 7: 17.
, : A new behavioral assessment scale for geriatric out- and in-patients: the NOSGER (Nurses’ Observation Scale for Geriatric Patients). J Am Geriatr Soc 1991; 39: 339–347.
: The Informant Questionnaire on Cognitive Decline in the Elderly (IQCODE): a review. Int Psychogeriatr 2004; 16: 275–293.
: Screening properties of the German IQCODE with a two-year time frame in MCI and early Alzheimer’s disease. Int Psychogeriatr 2010; 22: 91–100.
: Studies of illness in the aged: The Index of ADL: A standardized measure of biological and psychosocial function. JAMA 1963; 185: 914–919.
, .: An inventory to assess activities of daily living for clinical trials in Alzheimer’s disease. The Alzheimer’s Disease Cooperative Study. Alz Dis Assoc Disord 1997; 11: 33–39.
, : Neuropsychiatric Symptoms in Alzheimer’s disease. Alzheimers Dement 2011; 7: 532–539.
, : Empfehlungen zur Diagnostik und Therapie der behavioralen und psychologischen Symptome der Demenz (BPSD). Praxis 2014; 103: 135–148.
, : Development and validation of a geriatric depression screening scale: a preliminary report. J Psychiatr Res 1983; 17: 37–49.
: An inventory for measuring depression. Arch Gen Psychiatry 1961; 4: 53–63.
: American Psychiatric Association (APA): Diagnostisches und Statistisches Manual Psychischer Störungen DSM-5. 1: Hogrefe; 2015.
, : Dementia screening in general practice: Optimized scoring for the Clock Drawing Test. Brain Aging, 2002; 2: 36–43.
: Establishing robust cognitive dimensions for characterization and differentiation of patients with Alzheimer’s disease, mild cognitive impairment, frontotemporal dementia and depression. Int J Geriatr Psychiatry 2013; 29: 624–634.
: Systematic review of clinical prediction rules for neuroimaging in the evaluation of dementia. Arch Intern Med 2000; 160: 2855–2862.
: DEGAM – Leitlinie Nr. 12 DEMENZ 2008 Herausgeber: Deutsche Gesellschaft für Allgemeinmedizin und Familienmedizin (DEGAM), DEGAM,
Assessing dementia: the Canadian consensus . Organizing Committee, Canadian Consensus Conference on the Assessment of Dementia. CMAJ 1991; 144: 851–853., : Longitudinal rates of lobar atrophy in frontotemporal dementia, semantic dementia, and Alzheimer’s disease. Alzheimer Dis Assoc Disord 2010; 24: 43–48.
. Cognitive functioning in Alzheimer’s and vascular dementia: a meta-analysis. Neuropsychology 2009; 23: 411–423.
: Cerebral white matter lesions in patients with dementia – from MCI to severe Alzheimer’s disease. J Neurol Sci 2009; 283: 79–82.
, : (Hrsg.): Leitlinien für Diagnostik und Therapie in der Neurologie, Abschnitt: Diagnostik zerebrovaskulärer Erkrankungen. 4. Aufl. Stuttgart: Thieme; 2012.
, : Discrimination between Alzheimer dementia and controls by automated analysis of multicenter FDG PET. Neuroimage 2002; 17: 302–316.
: Alzheimer disease: operating characteristics of PET – a meta-analysis. Radiology 2004; 231: 73–80
, : Volume of interest-based [18F]fluorodeoxyglucose PET discriminates MCI converting to Alzheimer’s disease from healthy controls. A European Alzheimer’s Disease Consortium (EADC) study. Neuroimage Clin 2014; 7: 34–42.
, : Parallel ICA of FDG-PET and PiB-PET in three conditions with underlying Alzheimer’s pathology. Neuroimage Clin 2014; 4: 508–516.
, : Multicenter standardized 18F-FDG PET diagnosis of mild cognitive impairment, Alzheimer’s disease, and other dementias. J Nucl Med 2008; 49: 390–398.
: Diagnostic accuracy of ¹²³I-FP-CIT (DaTSCAN) in dementia with Lewy bodies: a meta-analysis of published studies. Parkinsonism Relat Disord 2012; 18: 225–229.
, : Neurotransmitter changes in dementia with Lewy bodies and Parkinson disease dementia in vivo. Neurology 2010; 74: 885–92.
, : Appropriate use criteria for Amyloid PET: a report of the Amyloid Imaging Task Force (AIT), the Society of Nuclear Medicine and Molecular Imaging (SNMMI) and the Alzheimer Association (AA). Alzheimers Dement 2013; 9: 1–16.
: Pharmacogenomics and therapeutic prospects in dementia. Eur Arch Psychiatry Clin Neurosci 2008; 258: 28–47.